El
metabolismo (del griego μεταβολή, cambio) es el conjunto de reacciones bioquímicas y procesos físico-
químicos que ocurren en una
célula y en el
organismo.
1 Estos complejos procesos interrelacionados son la base de la
vida a escala molecular, y permiten las diversas actividades de las células:
crecer,
reproducirse, mantener sus estructuras,
responder a estímulos, etc.
La metabolización es el proceso por el cual el organismo consigue que sustancias activas se transformen en no activas.
Este proceso lo realizan en los seres humanos con
enzimas localizadas en el
hígado. En el caso de las drogas psicoactivas a menudo lo que se trata simplemente es de eliminar su capacidad de pasar a través de las membranas de
lípidos, de forma que ya no puedan pasar la
barrera hematoencefálica, con lo que no alcanzan el sistema nervioso central.
Por tanto, la importancia del
hígado y el porqué este
órgano se ve afectado a menudo en los casos de consumo masivo o continuado de drogas.
El metabolismo se divide en dos procesos conjugados:
catabolismo y
anabolismo. Las
reacciones catabólicas liberan energía; un ejemplo es la
glucólisis, un proceso de degradación de compuestos como la
glucosa, cuya reacción resulta en la liberación de la energía retenida en sus enlaces químicos. Las
reacciones anabólicas, en cambio, utilizan esta
energía liberada para recomponer enlaces químicos y construir componentes de las células como lo son las
proteínas y los
ácidos nucleicos. El
catabolismo y el
anabolismo son procesos acoplados que hacen al metabolismo en conjunto, puesto que cada uno depende del otro.

Esquema de las principales rutas metabólicas
La economía que la actividad celular impone sobre sus recursos obliga a organizar estrictamente las reacciones químicas del metabolismo en vías o
rutas metabólicas, donde un compuesto químico (
sustrato) es transformado en otro (producto), y este a su vez funciona como sustrato para generar otro producto, siguiendo una secuencia de reacciones bajo la intervención de diferentes
enzimas(generalmente una para cada sustrato-reacción). Las
enzimas son cruciales en el metabolismo porque agilizan las reacciones físico-químicas, pues hacen que posibles reacciones
termodinámicasdeseadas pero "desfavorables", mediante un acoplamiento, resulten en reacciones favorables. Las enzimas también se comportan como factores reguladores de las vías metabólicas, modificando su funcionalidad –y por ende, la actividad completa de la vía metabólica– en respuesta al ambiente y necesidades de la célula, o según
señales de otras células.
Una característica del metabolismo es la similitud de las rutas metabólicas básicas incluso entre especies muy diferentes. Por ejemplo: la secuencia de pasos químicos en una vía metabólica como el
ciclo de Krebs es universal entre células vivientes tan diversas como la
bacteria unicelular Escherichia coli y
organismos pluricelulares como el
elefante. Esta estructura metabólica compartida es probablemente el resultado de la alta eficiencia de estas rutas, y de su temprana aparición en la historia evolutiva.
Clásicamente, el metabolismo se estudia por una aproximación centrada en una
ruta metabólica específica. La utilización de los diversos elementos en el organismo son valiosos en todas las categorías
histológicas, de
tejidos a células, que definen las rutas de precursores hacia su producto final.
6 Las enzimas que catabolizan estas reacciones químicas pueden ser purificadas y así estudiar su
cinética enzimática y las respuestas que presentan frente a diversos
inhibidores. Otro tipo de estudio que se puede llevar a cabo en paralelo es la identificación de los
metabolitos presentes en una célula o tejido; al estudio de todo el conjunto de estas moléculas se le denomina
metabolómica. Estos estudios ofrecen una visión de las estructuras y funciones de rutas metabólicas simples, pero son inadecuados cuando se quieren aplicar a sistemas más complejos como el metabolismo global de la célula.
7
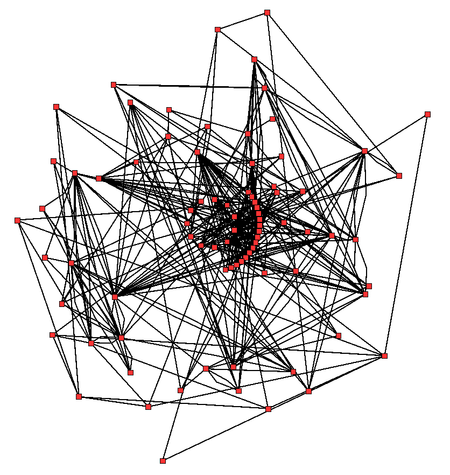
En la imagen de la derecha se puede apreciar la complejidad de una red metabólica celular que muestra interacciones entre tan sólo 43 proteínas y 40 metabolitos: esta secuencia de
genomas provee listas que contienen hasta 45.000
genes.
8 Sin embargo, es posible usar esta información para reconstruir redes completas de comportamientos bioquímicos y producir más modelos matemáticos
holísticos que puedan explicar y predecir su comportamiento.
9 Estos modelos son mucho más efectivos cuando se usan para integrar la información obtenida de las rutas y de los metabolitos mediante métodos clásicos con los datos de
expresión génica obtenidos mediante estudios de
proteómica y de
chips de ADN.
10
Una de las aplicaciones
tecnológicas de esta información es la
ingeniería metabólica. Con esta tecnología, organismos como las
levaduras, las
plantas o las
bacterias son modificados genéticamente para hacerlos más útiles en algún campo de la
biotecnología, como puede ser la producción de
drogas,
antibióticos o químicos industriales.
11 12 13 Estas modificaciones genéticas tienen como objetivo reducir la cantidad de energía usada para producir el producto, incrementar los beneficios y reducir la producción de desechos.
14

La
glucosa puede existir en forma de cadena y de anillo.
El metabolismo conlleva un gran número de reacciones químicas, pero la gran mayoría presenta alguno de los mecanismos de catálisis básicos de
reacción de transferencia en grupo.
24 Esta química común permite a las células utilizar una pequeña colección de intermediarios metabólicos para trasladar grupos químicos funcionales entre diferentes reacciones.
23 Estos intermediarios de transferencia de grupos son denominados
coenzimas. Cada clase de reacción de grupo es llevada a cabo por una coenzima en particular, que es el sustrato para un grupo de enzimas que lo producen, y un grupo de enzimas que lo consumen. Estas coenzimas son, por ende, continuamente creadas, consumidas y luego recicladas.
25
La coenzima más importante es el
adenosín trifosfato (ATP). Este
nucleótido es usado para transferir energía química entre distintas reacciones químicas. Sólo hay una pequeña parte de ATP en las células, pero como es continuamente regenerado, el cuerpo humano puede llegar a utilizar su propio peso en ATP por día.
25 El ATP actúa como una conexión entre el catabolismo y el anabolismo, con reacciones catabólicas que generan ATP y reacciones anabólicas que lo consumen. También es útil para transportar grupos fosfato en reacciones de
fosforilación.
Una
vitamina es un compuesto orgánico necesitado en pequeñas cantidades que no puede ser sintetizado en las células. En la
nutrición humana, la mayoría de las vitaminas trabajan como coenzimas modificadas; por ejemplo, todas las vitaminas hidrosolubles son fosforiladas o acopladas a nucleótidos cuando son utilizadas por las células.
26
La
nicotinamida adenina dinucleótido (
NAD), un derivado de la
vitamina B, es una importante coenzima que actúa como aceptor de protones. Cientos de deshidrogenasas eliminan
electrones de sus sustratos y
reducen el NAD
+ en NADH. Esta forma reducida de coenzima es luego un sustrato para cualquier componente en la célula que necesite reducir su sustrato.
27 El NAD existe en dos formas relacionadas en la célula, NADH y NADPH. El NAD
+/NADH es más importante en reacciones catabólicas, mientras que el NADP
+/NADPH es principalmente utilizado en reacciones anabólicas.

Estructura de la
hemoglobina. Las subunidades proteicas se encuentran señaladas en rojo y azul, y los grupos
hemode
hierro en verde.
Los elementos inorgánicos juegan un rol crítico en el metabolismo; algunos son abundantes (sodio y potasio, por ejemplo), mientras que otros actúan a concentraciones mínimas. Alrededor del 99% de la masa de un mamífero se encuentra compuesta por los elementos
carbono,
nitrógeno,
calcio,
sodio,
cloro,
potasio,
hidrógeno,
oxígeno y
azufre.
28 Los
compuestos orgánicos (proteínas, lípidos y carbohidratos) contienen, en su mayoría, carbono y nitrógeno, mientras que la mayoría del oxígeno y del hidrógeno están presentes en el agua.
28
Los
metales de transición se encuentran presentes en el organismo principalmente como
zinc y
hierro, que son los más abundantes.
3233 Estos metales son usados en algunas proteínas como
cofactores y son esenciales para la actividad de enzimas como la
catalasa y proteínas transportadoras del oxígeno como la
hemoglobina.
34 Estos
cofactores están estrechamente
ligados a una proteína; a pesar de que los cofactores de enzimas pueden ser modificados durante la
catálisis, siempre tienden a volver al estado original antes de que la catálisis tuviera lugar. Los
micronutrientes son captados por los organismos por medio de trasportadores específicos y proteínas de almacenamiento específicas tales como la
ferritina o la
metalotioneína, mientras no son utilizadas.
35 36
El conjunto de reacciones catabólicas más común en animales puede ser separado en tres etapas distintas. En la primera, moléculas orgánicas grandes como las proteínas, polisacáridos o lípidos son digeridos en componentes más pequeños fuera de las células. Luego, estas moléculas pequeñas son llevadas a las células y convertidas en moléculas aún más pequeñas, generalmente acetilos que se unen covalentemente a la
coenzima A, para formar la acetil-coenzima A, que libera energía. Finalmente, el grupo acetil en la molécula de
acetil CoA es oxidado a agua y dióxido de carbono, liberando energía que se retiene al reducir la coenzima
nicotinamida adenina dinucleótido (NAD
+) en NADH.
Los
microbios simplemente secretan enzimas digestivas en sus alrededores
39 40 mientras que los
animales secretan estas enzimas desde células especializadas al
aparato digestivo.
41 Los aminoácidos, monosacáridos, y triglicéridos liberados por estas enzimas extracelulares son absorbidos por las células mediante proteínas específicas de transporte.
42 43
El catabolismo de carbohidratos es la degradación de los
hidratos de carbono en unidades menores. Los carbohidratos son usualmente tomados por la célula una vez que fueron digeridos en monosacáridos.
44 Una vez dentro de la célula, la
ruta de degradación es la
glucólisis, donde los azúcares como la glucosa y la fructosa son transformados en
piruvato y algunas moléculas de ATP son generadas.
45 El piruvato o ácido pirúvico es un intermediario en varias rutas metabólicas, pero la mayoría es convertido en
acetil CoA y cedido al
ciclo de Krebs. Aunque más ATP es generado en el ciclo, el producto más importante es el NADH, sintetizado a partir del NAD
+ por la oxidación del acetil-CoA. La oxidación libera dióxido de carbono como producto de desecho. Una ruta alternativa para la degradación de la glucosa es la
ruta pentosa-fosfato, que reduce la coenzima
NADPH y produce azúcares de
5 carbonos como la
ribosa, el azúcar que forma parte de los
ácidos nucleicos.
Las grasas son catalizadas por la
hidrólisis a ácidos grasos y
glicerol. El glicerol entra en la glucólisis y los ácidos grasos son degradados por
beta oxidación para liberar acetil CoA, que es luego cedido al nombrado ciclo de Krebs. Debido a sus proporciones altas del grupo
metileno, los ácidos grasos liberan más energía en su oxidación que los carbohidratos, ya que los carbohidratos como la glucosa tienen más oxígeno en sus estructuras.
Los
aminoácidos son usados principalmente para sintentizar proteínas y otras biomoléculas; sólo los excedentes son oxidados a
urea y dióxido de carbono como fuente de energía.
46 Esta ruta oxidativa empieza con la eliminación del grupo amino por una
aminotransferasa. El grupo amino es cedido al
ciclo de la urea, dejando un esqueleto carbónico en forma de
cetoácido.
47 Los aminoácidos glucogénicos pueden ser transformados en glucosa mediante
gluconeogénesis.
48
Los protones bombeados fuera de la mitocondria crean una
diferencia de concentración a lo largo de la membrana, lo que genera un gradiente electroquímico.
51 Esta fuerza hace que vuelvan a la mitocondria a través de una subunidad de la
ATP-sintasa. El flujo de protones hace que la subunidad menor gire, lo que produce que el
sitio activo fosforile al
adenosín difosfato (ADP) y lo convierta en ATP.
25
La captura de
energía solar es un proceso similar en principio a la fosforilación oxidativa, ya que almacena
energía en
gradientes de concentración de protones, que da lugar a la síntesis de ATP.
25 Los electrones necesarios para llevar a cabo este transporte de protones provienen de una serie de proteínas denominadas
centro de reacción fotosintética. Estas estructuras son clasificadas en dos dependiendo de su
pigmento, siendo las bacterias quienes tienen un solo grupo, mientras que en las plantas y cianobacterias pueden ser dos.
60
En las plantas, el
fotosistema II usa energía solar para obtener los
electrones del agua, liberando oxígeno como producto de desecho. Los electrones luego fluyen hacia el
complejo del citocromo b6f, que usa su energía para bombear
protones a lo largo de la membrana
tilacoidea del
cloroplasto.
38 Estos protones se mueven a través de la ATP-sintasa, mediante el mismo mecanismo explicado anteriormente. Los electrones luego fluyen por el fotosistema I y pueden ser utilizados para reducir la coenzima
NADP+, que será utilizado en el
ciclo de Calvin, o recicladas para la futura generación de ATP.
61
El
anabolismo es el conjunto de procesos metabólicos constructivos en donde la energía liberada por el catabolismo es utilizada para sintetizar
moléculas complejas. En general, las moléculas complejas que dan lugar a estructuras celulares son construidas a partir de precursores simples. El anabolismo involucra tres facetas. Primero, la producción de precursores como
aminoácidos,
monosacáridos,
isoprenoides y
nucleótidos; segundo, su activación en
reactivos usando energía del ATP; y tercero, el conjunto de estos precursores en moléculas más complejas como
proteínas,
polisacáridos,
lípidos y
ácidos nucleicos.
Los organismos difieren en cuántas moléculas pueden sintetizar por sí mismos en sus células. Los
organismos autótrofos, como las plantas, pueden construir moléculas orgánicas complejas y proteínas por sí mismos a partir moléculas simples como dióxido de carbono y agua. Los
organismos heterótrofos, en cambio, requieren de una fuente de sustancias más complejas, como monosacáridos y aminoácidos, para producir estas moléculas complejas. Los organismos pueden ser clasificados por su fuente de energía:
- Fotoautótrofos y fotoheterótrofos, que obtienen la energía del Sol.
- Quimioheterótrofos y quimioautótrofos, que obtienen la energía mediante reacciones oxidativas.
La fotosíntesis es la síntesis de glucosa a partir de energía solar, dióxido de carbono (CO
2) y agua (H
2O), con oxígeno como producto de
desecho. Este proceso utiliza el ATP y el NADPH producido por los centros de reacción fotosintéticos para convertir el CO
2 en 3-fosfoglicerato, que puede ser convertido en glucosa. Esta reacción de fijación del CO
2 es llevada a cabo por la enzima
RuBisCO como parte del
ciclo de Calvin.
62 Se dan tres tipos de fotosíntesis en las plantas; fijación del carbono C3,
fijación del carbono C4 y
fotosíntesis CAM. Estos difieren en la vía que el CO
2 sigue en el ciclo de Calvin, con plantas C3 que fijan el CO
2 directamente, mientras que las fotosíntesis C4 y CAM incorporan el CO
2 en otros compuestos primero como adaptaciones para soportar la luz solar intensa y las condiciones secas.
63
En procariotas fotosintéticas, los mecanismos de la fijación son más diversos. El CO
2 puede ser fijado por el ciclo de Calvin, y asimismo por el
Ciclo de Krebs inverso,
64 o la carboxilación del
acetil-CoA.
65 66 Los quimioautótrofos también pueden fijar el CO
2 mediante el ciclo de Calvin, pero utilizan la energía de compuestos inorgánicos para llevar a cabo la reacción.
67
En el anabolismo de carbohidratos, se pueden sintetizar ácidos orgánicos simples desde
monosacáridos como la glucosa y luego sintetizar
polisacáridos como el
almidón. La generación de glucosa desde compuestos como el
piruvato, el
ácido láctico, el
glicerol y los
aminoácidos es denominada
gluconeogénesis. La gluconeogénesis transforma piruvato en glucosa-6-fosfato a través de una serie de intermediarios, muchos de los cuales son compartidos con la
glucólisis.
45 Sin embargo, esta ruta no es simplemente la inversa a la glucólisis, ya que varias etapas son catalizadas por enzimas no glucolíticas. Esto es importante a la hora de evitar que ambas rutas estén activas a la vez dando lugar a un ciclo fútil.
68 69
A pesar de que la
grasa es una forma común de almacenamiento de energía, en los
vertebrados como los
humanos, los
ácidos grasos no pueden ser transformados en glucosa por gluconeogénesis, ya que estos organismos no pueden convertir acetil-CoA en piruvato.
70 Como resultado, tras un tiempo de
inanición, los vertebrados necesitan producir
cuerpos cetónicosdesde los ácidos grasos para reemplazar la glucosa en tejidos como el
cerebro, que no puede metabolizar ácidos grasos.
71 En otros organismos como las plantas y las bacterias, este problema metabólico es solucionado utilizando el ciclo del glioxilato, que sobrepasa la
descarboxilación en el ciclo de Krebs y permite la transformación de acetil-CoA en ácido oxalacético, el cual puede ser utilizado en la síntesis de glucosa.
72 70
Los polisacáridos y los glicanos son sintetizados por medio de una adición secuencial de monosacáridos llevada a cabo por glicosil-transferasas de un donador reactivo azúcar-fosfato a un aceptor como el
grupo hidroxilo en el polisacárido que se sintetiza. Como cualquiera de los grupos hidroxilos del anillo de la
sustancia puede ser aceptor, los polisacáridos producidos pueden tener estructuras ramificadas o lineales.
73 Estos polisacáridos producidos pueden tener funciones metabólicas o estructurales por sí mismos o también pueden ser transferidos a lípidos y proteínas por medio de enzimas.
74 75
Ácidos grasos, isoprenoides y esteroides[editar · editar código]

Versión simplificada de la síntesis de
esteroides con los intermediarios de IPP (Isopentenil pirofosfato), DMAPP (Dimetilalil pirofosfato), GPP (Geranil pirofosfato) y
escualeno. Algunos son omitidos para mayor claridad.
Los ácidos grasos se sintentizan al polimerizar y reducir unidades de acetil-CoA. Las cadenas en los ácidos grasos son extendidas por un ciclo de reacciones que agregan el grupo acetil, lo reducen a
alcohol,
deshidratan a un grupo
alqueno y luego lo reducen nuevamente a un grupo
alcano. Las enzimas de la síntesis de ácidos grasos se dividen en dos grupos: en los animales y
hongos, las reacciones de la síntesis son llevadas a cabo por una sola proteína multifuncional tipo I,
76 mientras que en
plástidos de plantas y en bacterias son las enzimas tipo II por separado las que llevan a cabo cada etapa en la ruta.
77 78
Los
terpenos e
isoprenoides son clases de lípidos que incluyen carotenoides y forman la familia más amplia de productos naturales de la planta.
79 Estos compuestos son sintentizados por la unión y modificación de unidades de
isopreno donadas por los precursores reactivos pirofosfosfato isopentenil y pirofosfato dimetilalil.
80 Estos precursores pueden sintentizarse de diversos modos. En animales y
archaeas, estos compuestos se sintentizan a partir de acetil-CoA,
81 mientras que en plantas y bacterias se hace a partir de piruvato y gliceraldehído 3-fosfato como sustratos.
82 80 Una reacción que usa estos donadores isoprénicos activados es la biosíntesis de
esteroides. En este caso, las unidades de isoprenoides son unidas covalentemente para formar escualeno, que se pliega formando una serie de anillos dando lugar a una molécula denominada lanosterol.
83 El lanosterol puede luego ser transformado en esteroides como el
colesterol.
La habilidad de los organismos para sintetizar los 20 aminoácidos conocidos varía. Las bacterias y las plantas pueden sintetizar los 20, pero los mamíferos pueden sintetizar solo los diez aminoácido no esenciales.
17 Por ende, los
aminoácidos esencialesdeben ser obtenidos del alimento. Todos los aminoácidos son sintetizados por intermediarios en la glucólisis y el ciclo de Krebs. El nitrógeno es obtenido por el
ácido glutámico y la
glutamina. La síntesis de aminoácidos depende en la formación apropiada del ácido alfa-keto, que luego es
transaminado para formar un aminoácido.
84
Los aminoácidos son sintetizados en proteínas al ser unidos en una cadena por
enlaces peptídicos. Cada proteína diferente tiene una secuencia única e irrepetible de aminoácidos: esto es la
estructura primaria. Los aminoácidos pueden formar una gran variedad de proteínas dependiendo de la secuencia de estos en la proteína. Las proteínas son constituidas por aminoácidos que han sido activados por la adición de un
ARNt a través de un enlace
éster.
85 El aminoacil-ARNt es entonces un sustrato para el
ribosoma, que va añadiendo los residuos de aminoácidos a la cadena proteica, sobre la base de la secuencia de información que va
"leyendo" el ribosoma en una molécula de
ARN mensajero.